化学化合价怎么可以学好
2024-09-24 09:28:29
在化学中,化合价是一种元素的一个原子与其他元素的原子化合时表现出来的性质。
一、化合价确实定办法离子化合物在离子化合物中,化合价由元素的得失电子数决议。得到电子的元素显正价,失掉电子的元素显负价。例如,在氯化钠(NaCl)中,钠原子得到一个电子,显 + 1 价;氯原子失掉一个电子,显 - 1 价。共价化合物在共价化合物中,化合价由共用电子对的偏移方向决议。共用电子对倾向的元素显负价,偏离的元素显正价。例如,在水分子(H₂O)中,氢原子和氧原子共用电子对倾向氧原子,所以氢显 + 1 价,氧显 - 2 价。
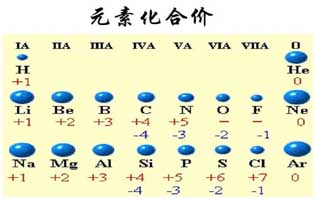
二、罕见元素的化合价一价元素氢(H)、锂(Li)、钠(Na)、钾(K)、银(Ag)等元素通常显 + 1 价。氟(F)、氯(Cl)、溴(Br)、碘(I)等元素通常显 - 1 价。二价元素铍(Be)、镁(Mg)、钙(Ca)、钡(Ba)、锌(Zn)等元素通常显 + 2 价。氧(O)在大少数化合物中显 - 2 价,但在过氧化物中(如过氧化氢 H₂O₂)显 - 1 价。三价元素铝(Al)、铁(Fe,在 + 3 价时)等元素通常显 + 3 价。
三、化合价的规律化合价有正有负金属元素通常显正价,非金属元素通常显负价,但也有一些非金属元素在某些化合物中显正价。例如,在二氧化硫(SO₂)中,硫显 + 4 价,氧显 - 2 价。单质的化合价爲零任何单质中元素的化合价都爲零。由于单质中元素的原子没有与其他元素的原子发作化合。化合物中各元素化合价代数和爲零在化合物中,一切元素化合价的代数和爲零。这是确定化合物中未知元素化合价的重要根据。例如,在硫酸(H₂SO₄)中,氢显 + 1 价,氧显 - 2 价,设硫的化合价爲,则,解得,所以硫显 + 6 价。
四、化合价的使用书写化学式依据化合价可以正确地书写高中化学必修1化合物的化学式。先确定化合物中各元素的化合价,然后依据化合价代数和爲零的准绳确定各元素原子的个数比。例如,已知铁显 + 3 价,氧显 - 2 价,要写出氧化铁的化学式,设氧化铁的化学式爲,则,令,,所以氧化铁的化学式爲₂₃。判别化学反响类型化合价的变化可以协助判别化学反响的类型。在氧化复原反响中,有元素的化合价发作变化;在非氧化复原反响中,一切元素的化合价都不变。例如,在氢气复原氧化铜的反响₂₂中,氢元素的化合价从 0 价降低到 + 1 价,铜元素的化合价从 + 2 价降低到 0 价,所以这是一个氧化复原反响。